已知室温下H3PO4的Ka1=7.5×10-3,Ka2=6.2×10-8,Ka3=2.2×10-13,
的有关信息介绍如下:H2PO4-的电离常数为bai6.2*10-8,水解常du数zhi为Kw/K1=1.33*10-12,电离大於水解所以dao是酸性。HPO42-的电离常数为zhuan2.2*10-13,水解常数为Kw/K2=1.61*10-7,水解大於电离所shu以是碱性。
解析:
电离常数等于溶液中的电离出来的各离子浓度乘积与溶液中未电离的电解质分子浓度的比值。电离平衡常数是弱电解质在一定条件下电离达到平衡时,溶液中电离所生成的各种离子浓度以其在电离方程式中的计量数为幂的乘积,跟溶液中未电离分子的浓度以其在化学方程式中的计量数为幂的乘积,适用于弱电解质的计算。
扩展资料:
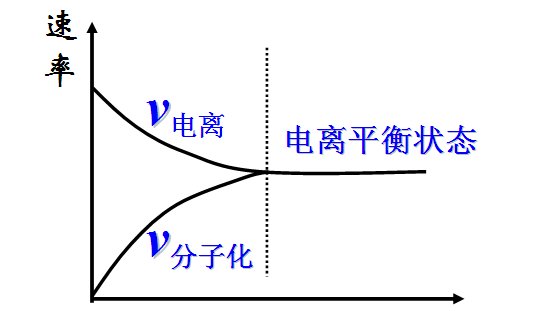
具有极性共价键的弱电解质(例如部分弱酸、弱碱)溶于水时,其分子可以微弱电离出离子;同时,溶液中的相应离子也可以结合成分子。一般地,自上述反应开始起,弱电解质分子电离出离子的速率不断降低,而离子重新结合成弱电解质分子的速率不断升高,当两者的反应速率相等时,溶液便达到了电离平衡。此时,溶液中电解质分子的浓度与离子的浓度分别处于稳定状态,不再发生变化。
用简单的语言概括电离平衡的定义,即:在一定条件下,弱电解质的离子化速率等于其分子化速率。
参考资料来源:百度百科—电离平衡常数



